- Natrium (Na): kraftig gul
- Kalium (K): svag lilla
- Kobber (Cu): grøn eller blågrøn
- Calcium (Ca): orange-rød
- Strontium (Sr): kraftig rød
- Barium (Ba): gulgrøn
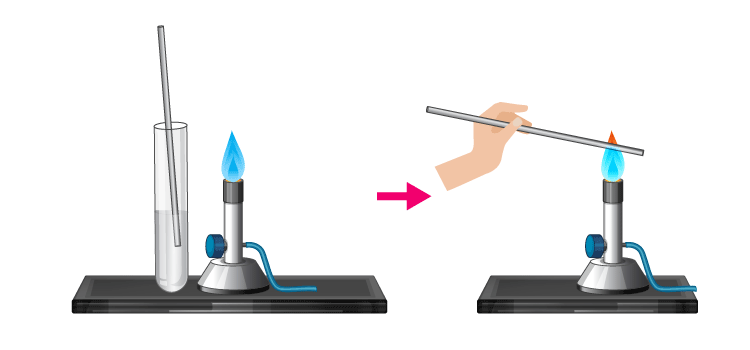 Forsøg
Forsøg
Til flammeprøven/analysen skal bruges:
- Gasbrænder
- Porcelænskål
- Kanthaltråd 0,5 mm eller en nikkelspatel.
- En bidtang
Ukendte stoffer f.eks.:
- Natriumchlorid, NaCl
- Lithiumchlorid, LiCl
- Kaliumchlorid, KCl
- Kobberchlorid, CuCl2
(Man kan som billederne viser også bruge sulfater og nitrater)
- En gasbrænder opspændes på skrå, så den øverste del befinder sig lige over en porcelænskål med vand. Indstil gasbrænderen så at den brænder med en blå-lig flamme.
- Afklip ca. 10 cm af kanthaltråden. Buk et lille øje i den ene ende af tråden.
- Til hver prøve skal bruges et nyt stykke kanthaltråd.
- Gennemglød det ombukkede øje grundigt i den øverste del af gasflammen, indtil den ikke længere farver flammen.
- Dyp hurtigt det varme trådøje i et af de ukendte stoffer, så der hænger lidt pulver ved.
- Hold derefter atter trådøjet ind i flammen og læg mærke til, hvilken flammefarve der fremkommer.
- Noter i et skema både flammefarven og det grundstof der måtte være i det ukendte stof.
Ved at lave en flammeprøve kan man altså bestemme hvilke grundstof der er i en prøve.
Analysen kan uddybes ved at benytte et spektroskop. Spektroskopet opdeler farverne i nogle linier eller bånd og hvert grundstof har sin egen specielle farvekombination (spektrum). Ved at se på flammefarven igennem spektroskopet vil grundstoffet kunne identificeres.
Metoden kaldes spektralanalyse.
Eksempler på farver der fremkommer ved forskellige grundstoffer
| Metal | Farve | |||
|
Kobber
|
grøn
|
kobberclorid,CuCl2
|
kobbersulfat, CuSO4
|
kobbernitrat, Cu(NO3)2
|
|
Natrium
|
stærk gul
|
natriumclorid, NaCl
|
natruimsulfat, Na2SO4
|
natriumnitrat, NaNO3
|
|
Calcium
|
orange
|
calciumclorid, CaCl2
|
calciumsulfat, CaSO4
|
Calciumnitrat, Ca(NO3)2
|
|
Kalium
|
lys violet
|
kaliumclorid, KCl
|
kaliumsulfat, K2SO4
|
kaliumnitrat, KNO3
|
|
Lithium
|
mørkrød
|
lithiumclorid, LiCl
|
lithiumsulfat, Li2SO4
|
lithiumnitrat, LiNO3
|












